بسم الله الرحمن الرحيم
السلام عليكم ورحمة الله وبركاته
حل أسئلة الفصل الثاني – المادة – الخواص والتغيرات
نبدأ على بركة الله ...
2-1
إتقان المفاهيم
31. اذكر ثلاثة أمثلة على مواد كيميائية نقية، وبين لماذا هي نقية؟
الحل:
الأكسجين والماء وكلوريد الصوديوم. مواد نقية لها تركيب ثابت ومنتظم لا يتغير العينات من مكان لآخر.
32. هل ثاني أكسيد الكربون مادة كيميائية نقية؟ ولماذا؟
الحل:
نعم، مادة نقية لأن له تركيب ثابت ومنتظم.
33. اذكر ثلاث خواص فيزيائية للماء.
الحل:
الماء مادة عديمة اللون، درجة غليان الماء 100 سليزيوس، درجة الانصهار صفر سليزيوس.
34. أي الخواص الآتية مميزة للمادة؟ وأيها غير مميزة؟
a. درجة الانصهار.
b. الكتلة.
c. الكثافة.
d. الطول.
الحل:
a. درجة الانصهار (خاصية مميزة).
b. الكتلة (خاصية غير مميزة).
c. الكثافة (خاصية مميزة).
d. الطول (خاصية غير مميزة).
35. هل العبارة الآتية صحيحة أم لا؟ علل إجابتك. "لا تتأثر الخواص بالضغط ودرجة الحرارة".
الحل:
العبارة غير صحيحة لأن الخواص الفيزيائية مثل الضغط والحرارة تؤثر على الخواص الكيميائية وقد تغير من المادة.
36. اذكر حالات المادة الثلاث، وأعط أمثلة عليها.
الحل:
حالات المادة الثلاثة هي الحالة الصلبة مثل الجليد والخشب، الحالة السائلة مثل الماء والحليب، الحالة الغازية مثل بخار الماء والأكسجين.
37. صنف المواد الآتية إلى صلبة أو سائلة أو غازية في ضوء حالاتها في درجات الحرارة العادية: الحليب، الهواء، النحاس، الهيليوم، الماس، الشمع.
الحل:
الحليب سائل، الهواء غاز، النحاس صلب، الهيليوم غاز، الماس صلب، الشمع صلب.
38. صنف الخواص الآتية إلى فيزيائية أو كيميائية.
a. للألومنيوم لون فضي.
b. كثافة الذهب 19g/cm3.
c. يشتعل الصوديوم عند وضعه في الماء.
d. يغلي الماء عند 100˚C.
e. تتكون طبقة سوداء على الفضة.
f. الزئبق سائل في درجات الحرارة العادية.
الحل:
a. للألومنيوم لون فضي (خاصية فيزيائية).
b. كثافة الذهب 19g/cm3 (خاصية فيزيائية).
c. يشتعل الصوديوم عند وضعه في الماء (خاصية كيميائية).
d. يغلي الماء عند 100˚C (خاصية فيزيائية).
e. تتكون طبقة سوداء على الفضة (خاصية كيميائية).
f. الزئبق سائل في درجات الحرارة العادية (خاصية فيزيائية).
39. فرغت علبة حليب في وعاء. صف التغيرات الحادثة في شكل الحليب وحجمه نتيجة ذلك.
الحل:
عند نقل الحليب إلى الوعاء يتخذ الحليب نفس شكل الوعاء الموجود فيه ولكن يظل حجم الحليب ثابت لا يتغير.
40. درجة الغليان عند أي درجة حرارة يغلي 250ml من الماء، و1000ml من الماء؟ هل درجة غليان الماء خاصية مميزة أم غير مميزة؟
الحل:
كلا من العينتين يغليان عند درجة حرارة واحدة لأن درجة الغليان خاصية فيزيائية مميزة للماء فأي عينة ماء تغلي عند درجة حرارة واحدة وهي 100 سليزيوس.
إتقان حل المسائل
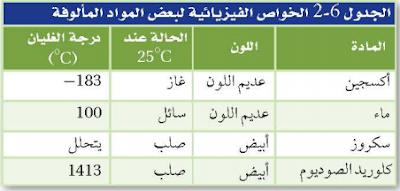
41. التحليل الكيميائي أراد عالم أن يعين مادة مجهولة بناء على خواصها الفيزيائية. المادة لونها أبيض، ولم تفلح المحاولات في تحديد درجة غليانها. استعمل الجدول 6-2 أدناه لتسمي هذه المادة.
الحل:
مادة صلبة بيضاء لذلك فهي سكروز أو كلوريد الصوديوم، ولكن المادة لا يستطيع تحديد درجة الغليان لأنها تتحلل لذلك فهي مادة السكروز.
2-2
إتقان المفاهيم
42. صنف كلا من التغيرات الآتية إلى كيميائي أو فيزيائي:
a. كسر قلم جزأين.
b. تجمد الماء وتكوين الجليد.
c. قلي البيض.
d. حرق الخشب.
e. تغير لون ورق الشجر في فصل الخريف.
الحل:
a. كسر قلم جزأين (تغير فيزيائي).
b. تجمد الماء وتكوين الجليد (تغير فيزيائي).
c. قلي البيض (تغير كيميائي).
d. حرق الخشب (تغير كيميائي).
e. تغير لون ورق الشجر في فصل الخريف (تغير كيميائي).
43. هل يعد تخمر الموز عملية فيزيائية أم كيميائية؟ فسر ذلك.
الحل:
تغير كيميائي لأنه حدث تغير في تركيب الموز وتكون نتائج جديدة لذلك فهو تغير كيميائي.
44. هل يعد تغير حالة المادة عملية فيزيائية أم كيميائية؟ فسر ذلك.
الحل:
تغير حالة المادة عملية فيزيائية لأنه لا يحدث أي تغير في تركيب المادة وإنما تتحول من شكل لشكل آخر.
45. اذكر أربعة مؤشرات على حدوث التفاعل الكيميائي.
الحل:
· تغير اللون.
· تصاعد غاز.
· تغير الطعم والرائحة.
· تحلل المواد.
46. صدأ الحديد يتحد الحديد مع الأكسجين في وجود بخار الماء لتكوين أكسيد الحديد، أو ما يعرف بصدأ الحديد. ما المواد المتفاعلة، وما المواد الناتجة؟
الحل:
المواد المتفاعلة هي الحديد والأكسجين وبخار الماء، المواد الناتجة هي أكسيد الحديد المصدئ أو كما يعرف بصدأ الحديد.
47. بعد أن اشتعلت شمعة مدة ثلاث ساعات بقي نصفها. وضح لماذا لا يخالف هذا المثال قانون حفظ الكتلة؟
الحل:
نصف الشمعة المحترقة تحولت لغازات متصاعدة وطاقة حرارية لذلك لا تتعارض مع قانون حفظ الكتلة لأن هنا تحولت الكتلة من مادة لمادة أخرى مع حفظها.
48. وضح الفرق بين التغير الفيزيائي والتغير الكيميائي.
الحل:
· التغير الفيزيائي هو تغير في مظهر المادة، ولكن يظل تركيبها الكيميائي ثابت لا يتغير مثل تشكيل صفيحة نحاس لكرة، تحول الجليد لماء، تكسير لوح زجاجي.
· التغير الكيميائي هو تحول المادة إلى مادة جديدة مختلفة التركيب والخواص وذلك بحدوث تفاعل كيميائي لها. وهناك أدلة على حدوث التغيير الكيميائي منها تغير اللون، تغير الطعم والرائحة وتغيير الخواص الفيزيائية مثل الكثافة والانجذاب للمغناطيس.
إتقان حل المسائل
49. إنتاج الأمونيا تفاعل 28.0g من النيتروجين كلياً مع 6.0g هيدروجين. ما كتلة الأمونيا الناتجة؟
الحل:
طبقاً لقانون حفظ الكتلة فإن كتلة المتفاعلات = كتلة المركب الناتج.
كتلة المتفاعلات = كتلة الهيدروجين + كتلة النيتروجين
= 6 + 28 = 34 جم.
كتلة الأمونيا النهائية = 34 جم.
50. تفاعل 45.98g صوديوم مع كمية زائدة من غاز الكلور، فنتج 116.89g من كلوريد الصوديوم. ما كتلة غاز الكلور الذي استهلك في هذا التفاعل؟
الحل:
طبقاً لقانون حفظ الكتلة فإن كتلة المتفاعلات = كتلة المركب الناتج.
كتلة كلوريد الصوديوم = 116.89 جم.
كتلة المتفاعلات = كتلة الصوديوم + كتلة الكلور
= 54.89 + كتلة الكلور = 116.89 جم
كتلة الكلور = 116.89 – 54.89 = 70.91 جم كلور
51. تحلل مادة ما كتلتها 680.0g إلى عناصرها بالتسخين. ما مجموع كتل عناصرها بعد التسخين؟
الحل:
طبقاً لقانون حفظ الكتلة فإن كتلة المتفاعلات = كتلة النتائج.
يجب العلم أن الكتلة محفوظة لذلك كتلة المادة قبل التسخين = كتلة عناصرها بعد التسخين = 680 جم.
52. عند حرق 180.0g جلوكوز في وجود 192.0g أكسجين نتج ماء وثاني أكسيد الكوبون. فإذا كانت كتلة الماء الناتج 108.0g، فما كتلة ثاني أكسيد الكربون الناتج؟
الحل:
طبقاً لقانون حفظ الكتلة فإن كتلة المتفاعلات = كتلة النتائج.
كتلة المتفاعلات = كتلة الجلوكوز + كتلة الأكسجين
= 180 + 192 = 372 جم
كتلة النتائج = كتلة الماء + كتلة ثاني أكسيد الكربون
= 108 + كتلة ثاني أكسيد الكربون = 372 جم
كتلة ثاني أكسيد الكربون = 372 – 108 =264 جم ثاني أكسيد الكربون.
2-3
إتقان المفاهيم
53. صف خواص المخلوط.
الحل:
مزيج من مادتين نقيتين أو أكثر، كل مادة من المخلوط تحتفظ بخواصها، يمكن أن مخلوط متجانس أو مخلوط غير متجانس.
54. اذكر طريقة الفصل التي يمكن استعمالها لفصل المخاليط الآتية:
a. برادة الحديد والرمل.
b. الرمل والملح.
c. مكونات الحبر.
d. غازي الهيليوم والأكسجين.
الحل:
a. المغناطيس.
b. نذوب المخلوط في الماء فلا يذوب الرمل ويتم فصله بالترشيح أما محلول الماء والملح فيتم تسخينه ويتبخر الماء ويظل الملح.
c. الكروماتوجرافي.
d. تبريد الغازين وتحويلها لسائل ثم نعمل تقطير للسائل النتائج ويتم الفصل على أساس.
55. ما صحة العبارة الآتية: "المخلوط مادة ناتجة عن اتحاد مادتين أو أكثر كيميائياً"؟ فسر إجابتك.
الحل:
العبارة غير صحيحة لأن المخلوط هو مزيج مواد بطريقة فيزيائية ويمكن فصل المزيج إلى مكوناته مرة ثانية وليس هناك أي ارتباط كيميائي.
56. فيم يختلف المخلوط المتجانس عن المخلوط غير المتجانس؟
الحل:
· المخلوط المتجانس مخلوط له تركيب ثابت وتمتزج مكوناته بانتظام، لو أخذت عينة من أي جزء تجدها مثل الجزء الآخر، لا يمكنك التمييز بين مكوناتها مثل: السبائك المعدنية، العصائر.
· المخلوط غير المتجانس مخلوط لا تمتزج مكوناته وتركيبه غير منتظم يمكنك التمييز بين مكوناتها مثل: سلطة الخضار، عصير البرتقال الطبيعي.
57. ماء البحر مكون من ملح ورمل وماء. هل هو مخلوط متجانس أو غير متجانس؟ فسر إجابتك.
الحل:
مخلوط غير متجانس لأن يمكن تمييز بعض مكوناته وهي الرمل كما أن تركيبه غير منتظم لذلك فهو غير متجانس.
58. ما الكروماتوغرافيا؟ وكيف تعمل؟
الحل:
الكروماتوغرافيا هي طريقة لفصل مكونات المخلوط بالاعتماد على جاذبية كل مكون من مكونات المخلوط لسطح مادة معينة.
2-4
إتقان المفاهيم
59. عرف العنصر.
الحل:
العنصر: هو مادة كيميائية نقية لا يمكن تجزئتها إلى أجزاء أصغر بالطرق الفيزيائية والكيميائية وكل عنصر له رمز كيميائي وعدد ذري خاص به.
60. صحح العبارات الآتية:
a. العنصر مزيج من مركبين أو أكثر.
الحل:
العنصر مادة كيميائية نقية لا يمكن تجزئتها إلى أجزاء أصغر بالطرق الفيزيائية والكيميائية وكل عنصر له رمز كيميائي وعدد ذري خاص به.
b. عندما تذوب كمية السكر كلياً في الماء ينتج محلول غير متجانس.
الحل:
ينتج محلول متجانس.
61. ما أهم إسهامات العالم مندليف في الكيمياء؟
الحل:
صمم مندليف جدولاً نظم فيه العناصر الموجودة في ذلك الوقت على أساس التشابهة في الكتلة.
62. سم العناصر المكونة لكل من المواد الآتية:
a. ملح الطعام NaCl.
b. الإيثانول C2H2OH.
c. الأمونيا NH3.
d. البروم Br2.
الحل:
a. صوديوم وكلور.
b. كربون وهيدروجين وأكسجين.
c. هيدروجين ونيتروجين.
d. البروم فقط.
63. هل يمكن التمييز بين العنصر والمركب؟ كيف؟
الحل:
نعم يمكن التمييز بينهما. المركب يمكن تجزئته بطرق كيميائية صعبة إلى العناصر المكونة له أما العنصر فلا يمكن تبسيطه إلى أبسط ما هو عليه.
64. هل تختلف خواص المركب عن خواص العناصر المكونة له؟
الحل:
نعم تختلف خواص المركب عن خواص المواد المكونة له مثل اختلاف الماء عن مكونيه الأكسجين والهيدروجين.
65. ما القانون الذي يشير إلى أن المركب يتكون من العناصر نفسها متحدة بنسب كتلية ثابتة؟
الحل:
قانون النسب الثابتة.
66. ما النسبة المئوية بالكتلة للكربون في CO2 44.0g؟
الحل:
كتلة الكربون في ثاني أكسيد الكربون = 12 جم.
النسبة المئوية بالكتلة للكربون = (كتلة الكربون / كتلة ثاني أكسيد الكربون) × 100 = (44 /12) × 100 = 27.27% كربون.
67. صنف المركبات الواردة
في الجدول 7-2 إلى (1:1)، (2:2)، (1:2).
الحل:
1. 1:1.
2. 1:1.
3. 2:1.
4. 2:2.
إتقان حل المسائل
68. تحتوي عينة كتلتها 25.3g من مركب ما على 0.8g أكسجين. ما النسبة بالكتلة للأكسجين في المركب؟
الحل:
كتلة الأكسجين في العينة = 0.8 جم.
كتلة العينة = 25.3 جم.
النسبة المئوية بالكتلة للأكسجين = (كتلة الأكسجين / كتلة العينة) × 100
= (25.3 / 0.8) × 100 = 3.16% أكسجين.
69. يتحد الماغنسيوم مع الأكسجين لتكوين أكسيد الماغنسيوم. إذا تفاعل 10.57g ماغنسيوم تماماً مع 6.96g أكسجين فما النسبة المئوية بالكتلة للأكسجين في أكسيد الماغنسيوم؟
الحل:
طبقاً لقانون حفظ الكتلة فإن كتلة المتفاعلات = كتلة النتائج.
كتلة أكسيد الماغنسيوم = كتلة الأكسجين + كتلة الماغنسيوم
= 10.57 + 6.96 = 17.53 جم أكسيد ماغنسيوم.
كتلة الأكسجين في العينة = 6.96 جم.
كتلة العينة = 17.53 جم.
النسبة المئوية بالكتلة للأكسجين = (كتلة الأكسجين / كتلة العينة) × 100
= (17.53 /6.96) × 100 = 39.7 % أكسجين.
70. عند تسخين أكسيد الزئبق فإنه يتحلل إلى زئبق وأكسجين. إذا تحلل 28.4g من أكسيد الزئبق ونتج 2.0g أكسجين فما النسبة المئوية بالكتلة للزئبق في أكسيد الزئبق؟
الحل:
طبقاً لقانون حفظ الكتلة فإن كتلة المتفاعلات = كتلة النتائج.
كتلة أكسيد الزئبق المتحلل = كتلة الأكسجين + كتلة الزئبق.
كتلة الزئبق = كتلة أكسيد الزئبق المتحلل – كتلة الزئبق
= 28.4 – 2 = 26.4 جم زئبق.
النسبة المئوية بالكتلة للزئبق = (كتلة الزئبق / كتلة العينة) × 100
= (28.4 / 26.4) × 100 = 92.95 % زئبق.
71. يتحد الكربون مع الأكسجين ويكون مركبين، يحتوي الأول منهما على 4.82g كربون لكل 6.44g أكسجين، ويحتوي الثاني على 20.13g كربون لكل 53.7g أكسجين. ما نسبة الكربون إلى كتلة ثابتة من الأكسجين في المركبين المذكورين؟
الحل:
· المركب الأول:
معطيات:
كتلة الكربون = 4.82 جم.
كتلة الأكسجين = 6.44 جم.
كتلة الكربون: كتلة الأكسجين.
4.82 : 6.44
(نقسم الطرفين على كتلة الكربون وهي 4.82)
1 كربون: 1.33 أكسجين.
· المركب الثاني:
المعطيات:
كتلة الكربون = 20.13 جم.
كتلة الأكسجين = 53.7 جم.
كتلة الكربون: كتلة الأكسجين.
20.13: 53.7
(نقسم الطرفين على كتلة الكربون وهي 20.13)
1 كربون: 2.66 أكسجين.
لذلك نسبة الكربون إلى الأكسجين في المركب الأول: نسبة إلى الأكسجين في المركب الثاني
(1.33: 2.66)
= 2.
72. عينة كتلتها 100.0g من مركب ما تحتوي على 64.0g من الكلور. ما النسبة المئوية بالكتلة للكلور في المركب؟
الحل:
النسبة المئوية بالكتلة للكلور = (كتلة الكلور / كتلة العينة) × 100
= (100 / 64) × 100
= 64% كلور.
73. ما القانون الذي تستعمله لمقارنة CO مع Co2؟ فسر ذلك. دون اللجوء إلى أي حسابات، حدد أي المركبين يحتوي على نسبة مئوية بالكتلة أعلى للأكسجين.
الحل:
نستخدم قانون النسب المتضاعفة. النسبة المئوية الكتلية للأكسجين في ثاني أكسيد الكربون أكبر عدد مولات الكربون بها ضعف عدد المولات في أول أكسيد الكربون.
74. أكمل الجدول 8-2 الآتي:

الحل:
· CuO :
النسبة المئوية بالكتلة للأكسجين = (كتلة الأكسجين / كتلة العينة) × 100
= (84 / 16) × 100 = 19.04% أكسجين
كتلة النحاس = 84 – 16 = 68 جم نحاس.
· H2O:
النسبة المئوية بالكتلة للأكسجين = (كتلة الأكسجين / كتلة العينة) × 100
= (18 / 16) × 100 = 88.88% أكسجين
كتلة هيدروجين = 18 – 16 = 2 جم هيدروجين.
· H2O2:
النسبة المئوية بالكتلة للأكسجين = (كتلة الأكسجين / كتلة العينة) × 100
= (34 / 32) × 100 = 94.11% أكسجين
كتلة هيدروجين = 34 – 32 = 2 جم هيدروجين.
· Co:
النسبة المئوية بالكتلة للأكسجين = (كتلة الأكسجين / كتلة العينة) × 100
= (28 / 16) × 100 = 57.14% أكسجين
كتلة الكربون = 28 – 16 = 12 جم كربون.
· Co2:
النسبة المئوية بالكتلة للأكسجين = (كتلة الأكسجين / كتلة العينة) × 100
= (44 / 32) × 100 = 72.72% أكسجين
كتلة الكربون = 44 – 32 = 12 جم كربون.
مراجعة عامة
75. أي حالات المادة قابلة للانضغاط؟ وأيها غير قابلة للانضغاط؟ فسر إجابتك.
الحل:
الحالة الغازية هي الحالة الوحيدة القابلة للانضغاط بسبب المسافات البينية والتباعد الكبير بين الجزيئات، بينما الحالتين الصلبة والسائلة غير قابلتين للانضغاط بسبب التراص والمسافات البينية المحدودة بين الجزيئات لذلك غير قابلة للانضغاط.
76. صنف المخاليط الآتية إلى متجانسة أو غير متجانسة:
a. النحاس الأصفر (سبيكة من الخارصين والنحاس).
b. السلطة.
c. الدم.
d. مسحوق شراب مذاب في الماء.
الحل:
a. مخلوط متجانس.
b. مخلوط غير متجانس.
c. مخلوط متجانس.
d. مخلوط متجانس.
77. يتحد الفوسفور مع الهيدروجين ليكون الفوسفين. وفي هذا التفاعل يتحد 123.9g من الفوسفور مع كمية وافرة من الهيدروجين لإنتاج 129.9g فوسفين، وبعد انتهاء التفاعل بقي 310.0g من الهيدروجين غير متفاعل. ما كتلة الهيدروجين التي استعملت في هذا التفاعل؟ وما كتلة الهيدروجين قبل التفاعل؟
الحل:
طبقاً لقانون حفظ الكتلة فإن كتلة المتفاعلات = كتلة النتائج.
المعطيات:
كتلة الفوسفين الناتج = 129.9 جم.
كتلة الفوسفور المتفاعل = 123.9 جم.
كتلة الفسفور + كتلة الهيدروجين = كتلة الفوسفين.
123.9 + كتلة الهيدروجين = 129.9
كتلة الهيدروجين = 129.9 – 123.9 = 6 جم
كتلة الهيدروجين المستعملة في التفاعل = 6 جم.
كتلة الهيدروجين المتبقي = 310 جم
كتلة الهيدروجين قبل التفاعل = كتلة الهيدروجين المتبقي + كتلة الهيدروجين المستخدم في التفاعل = 310 + 6 = 316 جم
78. إذا كان لديك 100 ذرة من الهيدروجين، و100 ذرة من الأكسجين، فما عدد جزيئات الماء التي يمكن أن تكونها؟ هل تستعمل جميع الذرات الموجودة من كلا العنصرين؟ إذا كان الجواب لا، فما الذي يبقى؟
الحل:
1 مول من جزئ الماء يحتوي على 2 مول من الهيدروجين و 1 مول من الأكسجين. أي بنسبة 1:2، نفترض أن عدد المولات هو عدد الذرات.
لذلك لتكوين 50 جزئ من الماء نحتاج إلى 100 ذرة من الهيدروجين و50 ذرة من الأكسجين. لا يتم استعمال جميع الذرات الموجودة من العنصرين، ولكن يتبقى 50 ذرة من الأكسجين.
79. صنف المواد الآتية إلى مواد نقية، أو مخلوط متجانس، أو مخلوط غير متجانس:
a. الهواء.
b. الدخان.
c. التراب.
d. الماء النقي.
e. الترسبات.
f. الماء الموحل.
الحل:
a. مخلوط متجانس.
b. مخلوط غير متجانس.
c. مخلوط غير متجانس.
d. مخلوط متجانس.
e. مواد نقية.
f. مخلوط غير متجانس.
80. حدد ما إذا كان كل مما يأتي مخلوطاً متجانساً أم مخلوطاً غير متجانس، أم مركباً، أم عنصراً:
a. ماء الشرب النقي.
b. الماء المالح.
c. الهيليوم.
d. ماء البحر.
e. الهواء.
الحل:
a. مركب.
b. مخلوط متجانس.
c. عنصر.
d. مخلوط غير متجانس.
e. مخلوط متجانس.
81. الطبخ اذكر الخواص الفيزيائية للبيض قبل سلقه وبعده. بناء على ملاحظاتك، هل يحدث تغير فيزيائي أو تغير كيميائي عند سلق البيض؟ فسر إجابتك.
الحل:
البيضة قبل سلقها تتكون من بياض شفاف اللون لزج وصفار لزج ولكن بعد السلق بيكون البياض صلب والصفار صلب أيضاً ويعتبر هذا تغير كيميائي لأن درجة الحرارة أحدثت تغيير في تركيب البيضة.
82. البيتزا هل البيتزا مخلوط متجانس أو غير متجانس؟
الحل:
البيتزا مخلوط غير متجانس لأنه يمكن التمييز بين مكونات البيتزا وفصلها.
83. يتفاعل الصوديوم كيميائياً مع الكلور ليكون كلوريد الصوديوم. هل كلوريد الصوديوم مخلوط أو مركب؟
الحل:
كلوريد الصوديوم مركب لأنه نتج من اتحاد مادتين كيميائياً وبينهما روابط أيونية ويكون المركب الناتج مختلف في خواصه عن مكوناته ويصعب فصل المركب بالطرق الفيزيائية.
84. بين ما إذا كان اتحاد العناصر الآتية يؤدي إلى تكوين مركب أو مخلوط:
a. ماء → H2(g) + O2(g)
b. هواء → N2(g) + O2(g)
الحل:
a. اتحاد الهيدروجين والأكسجين لتكوين مركب الماء لأنه نتج عنه مادة جديدة لا يمكن فصلها بالطرق العادية.
b. أما غازي النيتروجين والأكسجين فهو مخلوط متجانس من الهواء.
التفكير الناقد
85. تفسير البيانات يحتوي مركب على عنصرين X وY. حللت أربع عينات (IV، III، II، I) ذات كتل مختلفة، ثم رسمت كميات العنصرين في كل عينة بيانياً كما في الشكل 22-2 أدناه.
a. ما العينات المأخوذة من المركب نفسه؟ كيف عرفت؟
الحل:
العينات المأخوذة من نفس المركب هي I, IV, III لأن النسب بينهما متساوية وهما على خط مستقيم في الرسم البياني لذلك فهما من نفس المركب.
b. ما النسبة تقريباً لكتلة X إلى كتلة Y في العينات من المركب نفسه؟
الحل:
النسبة لكتلة X إلى كتلة Y هي مقلوب الميل وتساوي النسبة بينهما في أي من المركبات الثلاثة التي تقع على خط مستقيم 1: 3.8.
c. ما النسبة تقريباً لكتلة X إلى كتلة Y في العينات التي ليست من المركب نفسه؟
الحل:
النسبة بين كتلة X وكتلة Y هي في حدود 1.93 :1 .
86. طبق الهواء خليط مكون من غازات كثيرة، ومنها النيتروجين والأكسجين والأرجون. هل يمكن استخدام عملية التقطير لفصل الغازات المكونة للهواء؟ فسر إجابتك.
الحل:
يمكن استخدام التقطير في حالة تجميد هذه الغازات وتحويلها إلى سوائل ويمكن فصل هذه السوائل بالتقطير نظراً لاختلاف درجة تبخر كل غاز.
87. تحليل هل يعد خروج الغاز من عبوة المشروب الغازي المفتوحة تغيراً فيزيائياً، أم تغيراً كيميائياً؟ فسر إجابتك.
الحل:
هو تغير فيزيائي بالنسبة لثاني أكسيد الكربون لأن تركيبه لم يختلف سواء في العبوة أو خارج العبوة، ولكن بالنسبة للمشروب الغازي نفسه خروج كميات كبيرة من ثاني أكسيد الكربون يغير من طعم المشروب ويؤدي إلى تغير كيميائي.
مسألة تحفيز
88. مركبات الرصاص عينة من مركب تحوي 4.46g من الرصاص لكل 1g من الأكسجين، وعينة أخرى كتلتها 68.54g تحوي 28.26g من الأكسجين. هل العينتان من المركب نفسه؟ فسر إجابتك.
الحل:
نحدد نسبة الرصاص والأكسجين في كل عينة ومن خلال النسبة نحدد :
العينة الأولى = نسبة الرصاص / نسبة الأكسجين = 4.46 /1 =4.46
العينة الثانية :
كتلة الرصاص = 68.54 – 28.26 = 40.28 جم.
كتلة الأكسجين = 28.26 جم
العينة الثانية = نسبة الرصاص / نسبة الأكسجين = 40.28 / 28.26 = 1.42.
النسب مختلفة لذلك فالعينة لمركبين مختلفين.
مراجعة تراكمية
89. ما الكيمياء؟
الحل:
هي فرع من فروع العلوم يهتم بدراسة المادة والتغيرات التي تطرأ عليها.
90. ما الكتلة؟
الحل:
الكتلة هي مقدار ما يحتويه الجسم من مادة.
تقويم إضافي
الكتابة في الكيمياء
91. العناصر المصنعة اختر أحد العناصر المصنعة واكتب تقريراً قصيراً عن تطوره. ناقش في التقرير الاكتشافات الحديثة، واكتب فيه أهم مراكز الأبحاث التي توصلت إلى هذا النوع من البحث، وصف فيه خصائص العنصر المصنع.
الحل:
متروك للطالب.
مقال قد يساعد الطالب.
أسئلة المستندات
الأصباغ فهم العلماء منذ زمن طويل خصائص العناصر والمركبات. كما استخدم الفنانون الكيمياء لتحضير الأصباغ من المواد الطبيعية. يوضح الجدول 9-2 بعض الأصباغ التي استخدمت قديماً.
92. a. قارن نسبة الكربون بالكتلة لكل من الفحم، والنيلة، والزنجار.
الحل:
نسبة الكربون في الفحم = 100% كربون.
نسبة الكربون في النيلة = (كتلة الكربون / كتلة جزئ نيلة) × 100
= (262.27 / 192) × 100 = 73.2% كربون.
نسبة الكربون في الزنجار = (كتلة الكربون / كتلة جزئ زنجار) × 100
= (221/ 12) × 100 = 5.4% كربون.
b. قارن نسبة الأكسجين بالكتلة لأكسيد الحديد الأحمر مع الأزرق المصري.
الحل:
نسبة الأكسجين في أكسيد الحديد الأحمر = (كتلة الأكسجين / كتلة جزئ أكسيد الحديد الأحمر) × 100
= (159.7 / 48) × 100 = 30 % أكسجين.
نسبة الأكسجين في الأزرق المصري = (كتلة الأكسجين / كتلة الأزرق المصري) × 100
= (375.5 / 160) × 100 = 42.6 % أكسجين.
93. اذكر مثالاً على عنصر ومثالاً على مركب، مستعيناً بالجدول 9-2 أعلاه.
الحل:
مثال على الفحم وهو يتكون من عنصر الكربون.
مثال على مركب أكسيد الحديد الأحمر.
94. هل يعد إنتاج الفحم بالتقطير الجاف للخشب تغيراً فيزيائياً أم تغيراً كيميائياً؟ فسر إجابتك.
الحل:
تغير كيميائي بسبب تغير تركيب الخشب الجاف لفحم فيتغير الروابط ولون الناتج.
تم بحمد الله
نستقبل أسئلتكم واستفساراتكم واقتراحاتكم في خانة التعليقات
"نرد على جميع التعليقات"
بالتوفيق للجميع...^-^










ليست هناك تعليقات:
إرسال تعليق